VILLOSITÉS INTESTINALES AVEC DES BACTÉRIES
Mesurer les Microbiomes
Historiquement, l'identification des micro-organismes reposait sur des méthodes de culture cellulaire. Cette méthode présente des limites importantes, notamment l'impossibilité de mettre en culture tous les organismes du microbiome.1-3
Tous les micro-organismes ne sont pas viables dans les conditions in vitro associées aux méthodes de culture cellulaire.1
Les méthodes moléculaires de nouvelle génération utilisent des séquences d'ADN bactérien comme substituts pour les organismes afin d'identifier leur taxonomie, leur abondance relative et leur fonction.1,4-6 Les méthodes les plus couramment utilisées sont brièvement décrites ci-dessous.
Présentation des méthodes couramment utilisées pour mesurer le microbiome
Séquençage de gènes marqueurs basé sur des amplicons
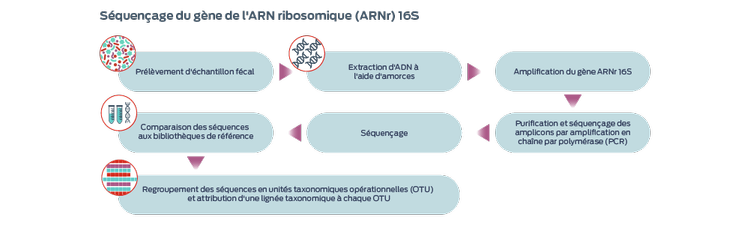
L'approche la plus couramment utilisée consiste à séquencer le gène de l'ARN ribosomique (ARNr) 16S, présent dans toutes les bactéries et archées, mais absent dans les champignons ou dans le règne animal, pour générer un recensement microbien de l'échantillon.1,4,7 L'identification du mycobiome utilise des substituts du gène d'ARNr 18S.7
Le gène de l'ARNr 16S est fortement conservé entre les espèces bactériennes mais comprend des régions hypervariables qui favorisent sa différenciation.1 Cette approche permet d'identifier de nombreux micro-organismes à partir d'un échantillon, notamment les micro-organismes qui se prêtent mal à la culture cellulaire.1 Toutefois, cette technique ne fait pas la distinction entre les micro-organismes vivants ou morts, transitoires ou résidents, commensaux ou pathogènes, ou résistants ou sensibles aux antibiotiques.1
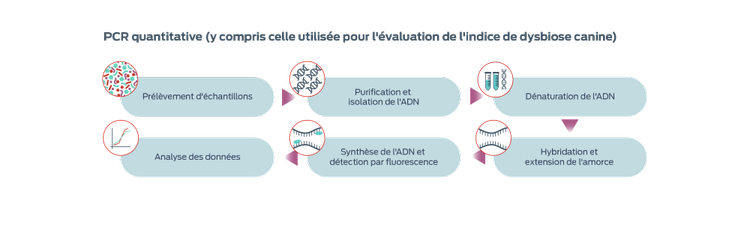
Réaction en chaîne par polymérase quantitative (PCR quantitative)
La PCR dite quantitative ou en temps réel est une méthode rapide et peu coûteuse permettant la quantification des taxons bactériens d'intérêt et le développement d'intervalles de référence. En s'appuyant sur la PCR quantitative pour sept espèces bactériennes, un indice de dysbiose du microbiote canin a ainsi pu être développé. Il permet de suivre les changements dans le microbiome en réponse au traitement.3
Ce lien renvoie à un article en anglais qui n'est pas disponible en français.
Description du « recensement microbien »
Les unités taxonomiques opérationnelles (OTU, pour Operational Taxonomic Units) sont des regroupements de séquences d'ADN effectués sur la base de leur similitude. Les séquences représentatives de chaque OTU sont comparées aux bases de données de référence pour attribuer l'identification des microbes dans le groupe.
La diversité alpha et la diversité bêta indiquent l'aire de répartition des espèces dans le microbiome. La diversité alpha est une mesure de la diversité au sein d'un échantillon.1 La diversité alpha tient compte de la richesse (le nombre d'espèces/OTU et leur répartition) et de l'uniformité (l'abondance relative des différentes OTU/espèces et leur répartition). La diversité alpha repose sur des algorithmes et s'exprime communément sous forme d'indice, comme l'indice de Shannon ou celui de Simpson.1 La diversité bêta est quant à elle une mesure de la dissimilarité entre les échantillons, souvent représentée sous forme de profils de groupes. Les systèmes utilisés pour calculer la diversité bêta sont le système Bray-Curtis et le système UniFrac non pondéré ou pondéré.1
Passage du recensement à la fonction
À mesure que la recherche avance, deux questions principales se posent concernant le microbiome : quels microbes sont présents, et quelle est leur fonction ? L'identification des micro-organismes présents dans le microbiome ne fournit pas d'informations sur leur fonction.3,5 Il est probable que certaines fonctions métaboliques et moléculaires soient exécutées par plus d'un microbe, ce qui donne lieu à un écosystème redondant offrant flexibilité et résilience.3,8
En raison de cette redondance, l'analyse du microbiome sur la base des espèces microbiennes présentes dans la population est insuffisante et ne permet donc pas de détecter les changements fonctionnels du microbiome. Bien que l'abondance relative des microbes puisse ou non être modifiée par une intervention ou une pathologie, le microbiome présent peut déplacer les activités microbiennes et le métabolisme pour compenser cette modification ; afin de détecter ces changements, différentes procédures analytiques sont nécessaires .
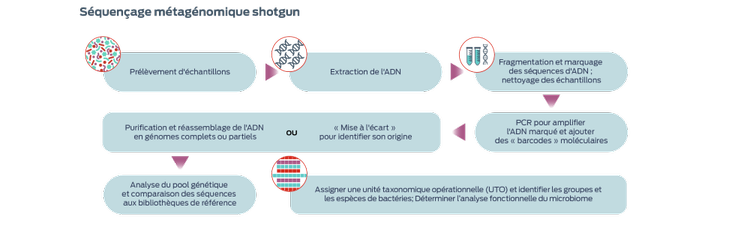
Séquençage métagénomique shotgun
Les méthodes « shotgun » (littéralement, « fusil de chasse » en anglais), ainsi nommées parce qu'elles ne sont pas ciblées (c'est-à-dire qu'elles ne sont pas destinées à détecter la présence d'un ensemble prédéterminé de microbes), gagnent en popularité dans l'analyse du microbiome des animaux de compagnie. Ces méthodes offrent l'avantage du séquençage des gènes fonctionnels, par opposition à la simple identification des bactéries.3-5 Toutefois, ces procédures nécessitent de plus grandes quantités d'ADN dans les échantillons et sont en outre plus coûteuses.3
Le séquençage « à longues lectures » facilite l'assemblage de génomes complets, y compris les gènes généralement manqués avec la métagénomique à « lectures courtes » et qui fournissent des informations biologiques supplémentaires.6
Métabolomique, protéomique et transcriptomique
Ces processus mesurent l'activité fonctionnelle dans un microbiome.4 Les méthodes de métabolomique sont utilisées pour déterminer le profil des métabolites, généralement caractérisé par des processus tels que la résonance magnétique nucléaire, la spectroscopie, la spectroscopie de masse et la chromatographie en phase liquide.7 Ces approches examinent les voies régulées par les microbes, comme la production d'acides gras volatils, le métabolisme des acides biliaires, la production de neutrotransmetteurs et la production d'indole.3

Explorer d'autres sections du Microbiome Forum

Interventions Portant sur le Microbiome pour Soigner les Pathologies des Animaux de Compagnie
En savoir plus
- Belas, A., Marques, C., & Pomba, C. (2020). The gut microbiome and antimicrobial resistance in companion animals. In Duarte, A. & Lopes da Costa, L. (Eds.), Advances in Animal Health, Medicine and Production (1st ed.), pp. 233—245. Springer International Publishing
- Cunningham, M., Azcarate-Peril, M. A., Barnard, A., Benoit, V., Grimaldi, R., Guyonnet, D.,…Gibson, G. R. (2021). Shaping the future of probiotics and prebiotics. Trends in Microbiology, 29(8), 667—685. doi:10.1016/j.tim.2021.01.003
- Pilla, R., & Suchodolski, J. S. (2021). The gut microbiome of dogs and cats, and the influence of diet. Veterinary Clinics of North America Small Animal Practice, 51(3), 605–621. doi:10.1016/j.cvsm.2021.01.002
- Bokulich, N. A., Ziemski, M., Robeson, M. S., & Kaehler, B. D. (2020). Measuring the microbiome: Best practices for developing and benchmarking microbiomics methods. Computational and Structural Biotechnology Journal, 18, 4048–4062. doi:10.1016/j.csbj.2020.11.049
- Radjabzadeh, D., Uitterlinden, A. G., & Kraaij, R. (2017). Microbiome measurement: Possibilities and pitfalls. Best Practice & Research Clinical Gastroenterology, 31, 619–623. doi:10.1016/j.bpg.2017.10.008
- Cusco, A., Pérez, D., Viñes, J., Fàbregas, N., & Francino, O. (2020). Long-read metagenomics retrieve complete single-contig bacterial genomes from canine feces. In review, BMC Genomics. doi:10.21203/rs.3.rs-135952/v1
- Marchesi, J. R. & Ravel, J. (2015). The vocabulary of microbiome research: a proposal. Microbiome, 3, 31. doi:10.1186/s40168-015-0095-5
- Koidl, L., & Untersmayr, E. (2021). The clinical implications of the microbiome in the development of allergy diseases. Expert Review of Clinical Immunology, 17, 115—126. doi:10.1080/1744666X.2021.1874353
